Lève-toi, et marche; c’est ce qu’auraient pu s’exclamer des chercheurs américains de l’université de Northwestern, qui ont récemment accompli un exploit quasiment biblique. Grâce à un tout niveau type de traitement, ils sont parvenus à soigner la paralysie de souris victimes de lésions de la moelle épinière en une seule injection !
Depuis des décennies, la science cherche à soigner la paralysie. C’est particulièrement compliqué, car contrairement à bon nombre de leurs semblables, les cellules du système nerveux central sont incapables de se régénérer seules. Cela comprend malheureusement la moelle épinière, avec des implications parfois terribles; lorsque celle-ci est très endommagée, la personne se retrouve souvent atteinte d’une paralysie irréversible.
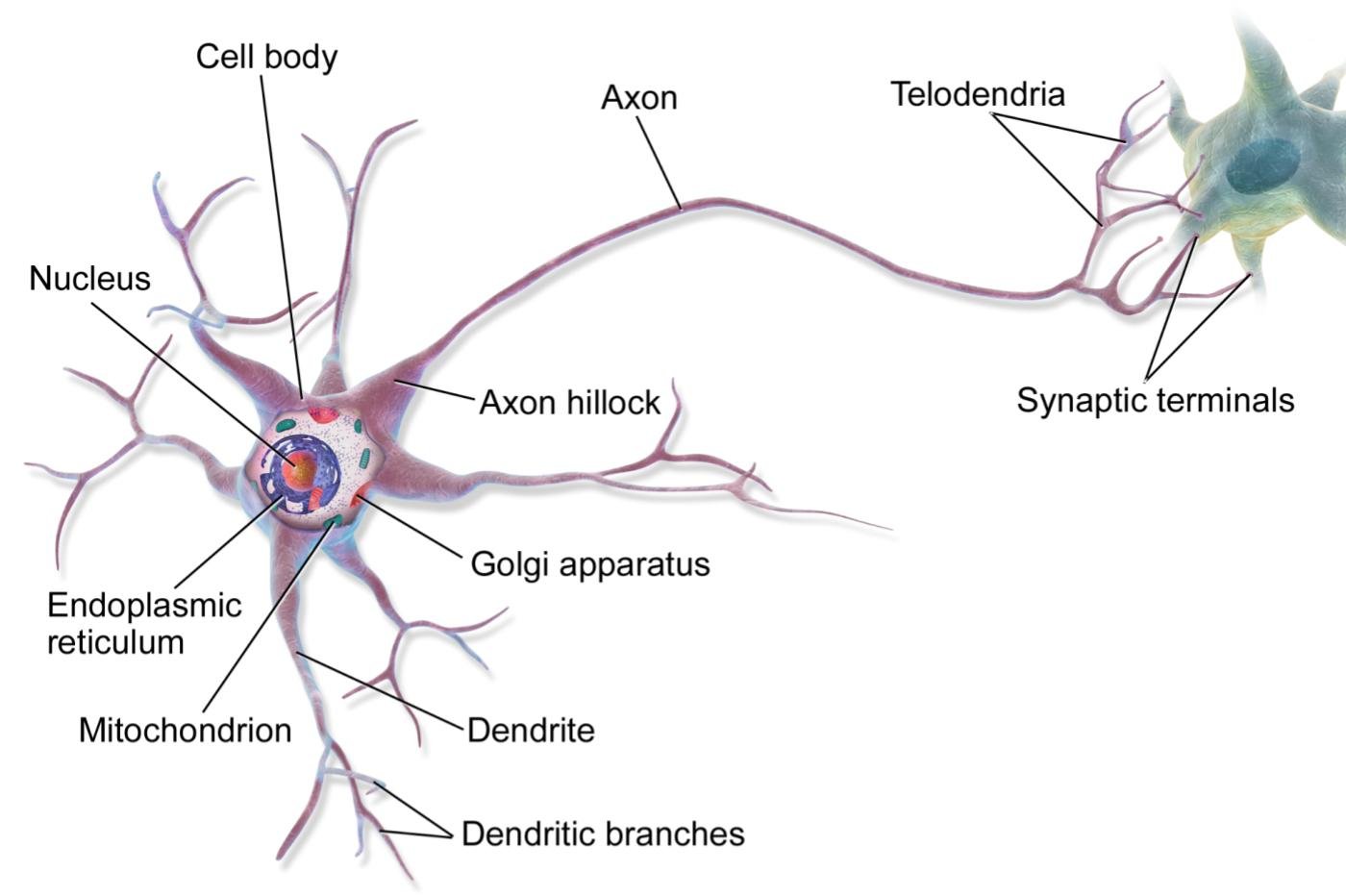
Cette conséquence est due à la structure de la moelle épinière. Comme le cerveau, elle est en partie composée de neurones. Ceux-ci sont légèrement différents de ceux du cerveau, mais fonctionnent de la même façon. En pratique, ils transmettent des informations sous forme de signal électrique, à travers un “câble” baptisé axone. Ce sont ces axones qui sont endommagés chez les personnes paralysées, et que la science cherche à réparer – bien souvent sans succès.
Un ballet de nanofibres “danseuses”
“Aujourd’hui, il n’y a aucune solution thérapeutique qui puisse déclencher la régénération de la moelle épinière”, explique Samuel I. Stupp, auteur principal de l’étude. Pour surmonter ce problème, de nombreux chercheurs ont déjà tenté des protocoles basés sur les cellules souches; une approche qui a déjà montré tout son potentiel en bio ingénierie et en médecine régénérative. Mais dans leurs travaux, publiés dans le prestigieux Science, cette équipe a opté pour une approche radicalement différente.
Plutôt que d’essayer de remplacer les neurones avec des cellules souches, ils ont misé sur un vaste réseau de nanofibres. Lorsque le traitement est injecté, ces nanofibres s’agglomèrent pour former un réseau dense et élastique. Celui-ci va jouer le rôle du tissu conjonctif, c’est-à-dire la partie structurelle de notre anatomie qui maintient tout le reste en place. Il sert ainsi d’ossature, un petit peu comme les barres d’acier dans une structure en béton armé.
Une fois cette structure de soutien en place, il reste la partie la plus difficile. Pour la réparation à proprement parler, les chercheurs ont choisi de faire d’une pierre de coup. Car les nanofibres en question ne servent pas seulement de tuteurs. Elles servent de maîtres de cérémonie au cours d’un ballet moléculaire extrêmement bien coordonné. Sous leur impulsion, des centaines de milliers de molécules avoisinantes se mettent en mouvement à la recherche d’un récepteur biologique bien précis.
Un signal chimique régénérateur
Une fois qu’elles ont trouvé leur récepteur, ces “molécules danseuses” se stabilisent et commencent à émettre un signal chimique. Celui-ci stimule à son tour la croissance des axones et des vaisseaux sanguins qui les alimentent, et ce sur une durée prolongée. Cela permet de rétablir progressivement la communication cellulaire entre les neurones, et donc de régénérer la moelle épinière.
Comme souvent en biologie animale, les cobayes ont été sacrifiés au terme de l’expérience. L’objectif : observer les changements au niveau cellulaire. Les chercheurs ont ainsi constaté que toutes les parties importantes des axones sectionnés s’étaient régénérées correctement. Cela confirme le succès de la manipulation à cette échelle. De plus, cela a permis de confirmer qu’il ne restait aucune trace de l’injection de départ; l’ensemble des fibres ont été biodégradées pour servir de nourriture aux cellules convalescentes.
Des applications thérapeutiques quasiment infinies
Ce n’est pas la toute première fois qu’une équipe de chercheurs rend l’usage de ses membres à une souris paralysée; cet honneur revient à une équipe de chercheurs allemands qui a publié ses travaux en janvier dernier. En revanche, c’est la toute première fois qu’un traitement permet de le faire de façon aussi fiable, rapide, et en une seule injection ponctuelle. De plus, cette approche laisse entrevoir des pistes d’amélioration très claires; c’est particulièrement important, car cela ouvre la porte à des solutions thérapeutiques concrètes.
Les chercheurs ont encore du pain sur la planche. Dans un premier temps, ils souhaitent améliorer encore davantage la capacité des fibres à trouver leur récepteur, ce qui accélérerait d’autant plus le traitement. Forts de leurs résultats extrêmement convaincants, ils espèrent désormais recevoir l’autorisation de passer directement à un essai clinique sur des humains. Dans un futur pas si lointain, nous pourrions donc voir arriver une vraie lueur d’espoir pour les 250.000 à 500.000 personnes qui souffrent de lésions de la moelle épinière chaque année dans le monde.
Mais le plus intéressant, c’est que les applications potentielles de cette technologie ne s’arrêtent pas à la paralysie. En théorie, il serait possible de soigner des tas de maladies graves liées au système nerveux central. Car fonctionnellement parlant, la structure réparée par les chercheurs est similaire à celles qui sont touchées dans le cadre de la maladie de Parkinson, d’Alzheimer ou de Charcot. Cerise sur le gâteau : les applications potentielles de ce système dépassent même le cadre du système nerveux. “Cette découverte fondamentale sur le contrôle des assemblages moléculaire pourraient être appliquées de façon universelles, à l’ensemble des cibles biomédicales“, conclut Stupp.
Le texte de l’étude est disponible ici.
🟣 Pour ne manquer aucune news sur le Journal du Geek, suivez-nous sur Google et sur notre canal WhatsApp. Et si vous nous adorez, on a une newsletter tous les matins.











