Comme chaque octobre, la semaine des Nobel s’est ouverte avec le prix de physiologie ou de médecine. Cette année, ce sont les chercheurs américains Mary E. Brunkow et Fred Ramsdell ainsi que le Japonais Shimon Sakaguchi qui ont été récompensés pour leurs travaux sur le contrôle du système immunitaire, cette délicate machinerie moléculaire qui permet à notre organisme de se défendre contre les assauts de son environnement.
Plus spécifiquement, les trois lauréats sont à l’origine de découvertes cruciales sur des acteurs particulièrement importants de ce système immunitaire : les lymphocytes.
Quand notre système immunitaire se retourne contre nous
Les membres les plus connus de cette famille sont les lymphocytes T CD8+, dits cytotoxiques ; ce sont de véritables tueurs à gages microscopiques dont le rôle est de se débarrasser des cellules endommagées ou malades, notamment lorsqu’elles deviennent cancéreuses ou sont infectées par des virus ou des bactéries.
Mais il arrive que ces tueurs à l’efficacité redoutable fassent des excès de zèle. Dans certains cas, ils peuvent se tromper de cible et décimer des cellules pourtant saines. Et c’est un gros problème, car cela ouvre la voie à des maladies auto-immunes aux conséquences potentiellement catastrophiques.
Heureusement, la plupart des gens ne sont pas touchés par ces maladies auto-immunes. Cela implique qu’il existe forcément un mécanisme capable d’imposer certaines limites à ces lymphocytes tueurs – et c’est un point qui a longtemps fait débat chez les spécialistes de la discipline.
Dans les années 1990, la plupart des spécialistes adhéraient à l’hypothèse de la « tolérance centrale », selon laquelle la tolérance immunitaire se construit avec l’élimination de cellules immunitaires hostiles dans le thymus.
Mais en 1995, Shimon Sakaguchi a mis un immense coup de pied dans la fourmilière en montrant que le tableau était nettement plus complexe. Il a notamment annoncé la découverte d’un nouveau type de cellule qui a bousculé l’ordre établi : les lymphocytes T CD4+, dits régulateurs.
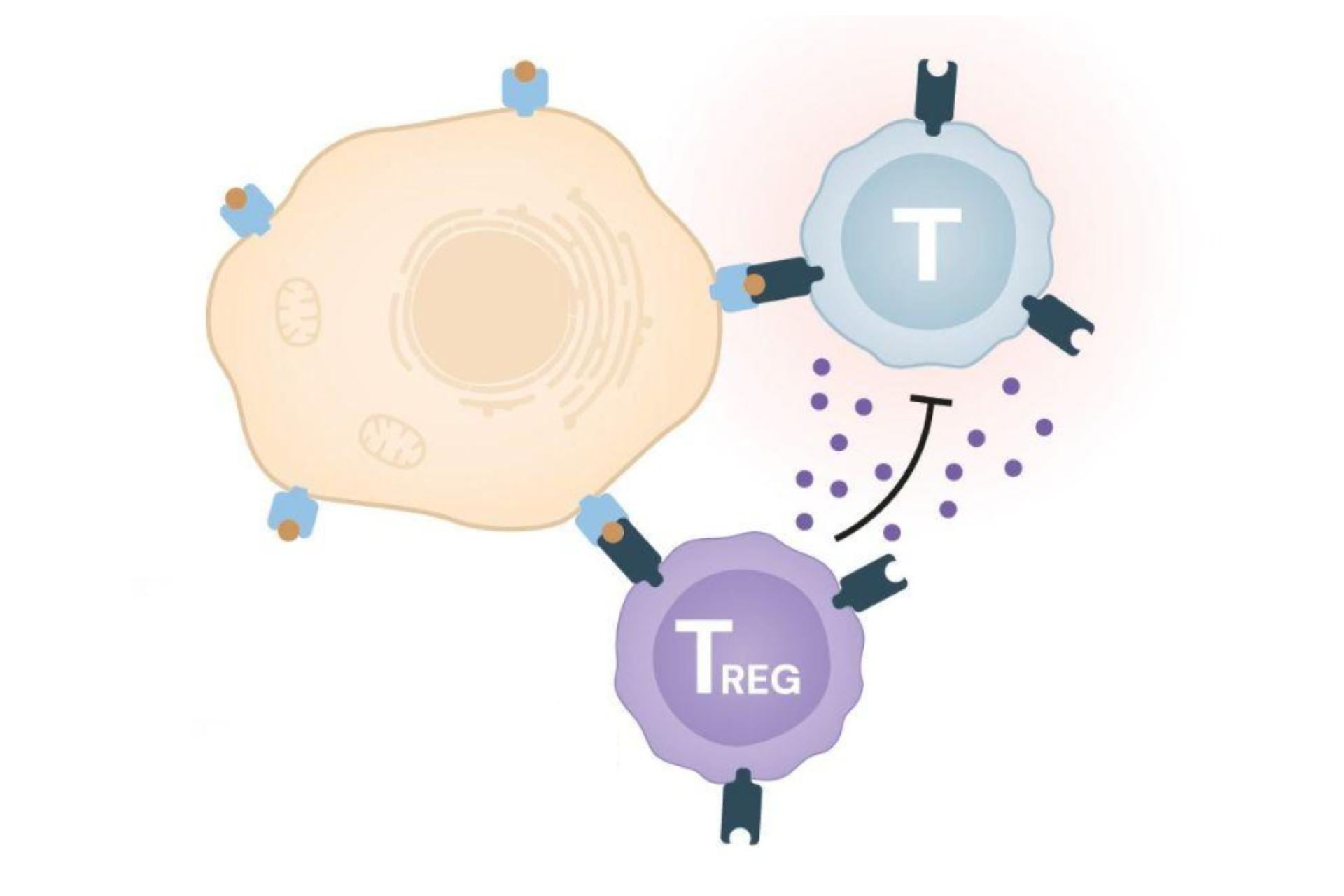
Il s’agit de cellules immunitaire originaires de la même lignée que les lymphocytes T cytotoxiques, mais avec une différence cruciale. Comme leur nom l’indique, elles sont spécialisées dans la régulation; leur rôle principal est de calmer les ardeurs de ces lymphocytes cytotoxiques pour éviter les dommages collatéraux lourds de conséquences.
La prochaine grande innovation est arrivée en 2001, avec les deux autres lauréats, Mary Brunkow et Fred Ramsdell. Ils ont été les premiers à montrer pourquoi certaines souris sont particulièrement vulnérables aux maladies auto-immunes. Il se trouve que ces rongeurs présentent une mutation sur un gène appelé Foxp3, et que l’équivalent humain de ce gène est directement responsable d’une maladie sérieuse, le syndrome IPEX.
Deux ans plus tard, Sakaguchi a réuni ces deux pièces du puzzle : il a réussi à prouver que le gène Foxp3 gouverne le développement des lymphocytes T régulateurs qu’il avait découverts en 1995.
Ces contributions se sont avérées essentielles à notre compréhension du fonctionnement de notre système immunitaire. Sur les vingt dernières années, ces travaux ont aussi eu des retombées très concrètes en médecine clinique ; c’est grâce à eux que d’autres chercheurs ont pu élaborer de nombreux traitements contre le cancer et diverses maladies auto-immunes graves.
En d’autres termes, les trois chercheurs ont non seulement contribué à éclaircir l’un des grands mystères de la biologie, mais ils ont aussi posé les bases d’autres travaux qui ont ensuite sauvé des millions de vies – un bilan qui méritait bien la plus prestigieuse des distinctions académiques.
Le cortège des Nobel continuera dès demain avec le prix de physique, qui sera attribué dans l’après-midi du mardi 7 octobre.
🟣 Pour ne manquer aucune news sur le Journal du Geek, suivez-nous sur Google et sur notre canal WhatsApp. Et si vous nous adorez, on a une newsletter tous les matins.











